Esta é a segunda parte duma série de artigos sobre o instrumento Near Infrared Mapping Spectrometer (NIMS), a bordo da sonda espacial americana Galileu, que se encontra em óbita do planeta Júpiter. Nesta parte explico o necessário sobre a espectroscopia, em particular de planetas, para se perceber como funciona NIMS, que tipo de dados fornece, e o que nos podem ensinar estes dados.
Espectros, uma explicação
 |  |
 | 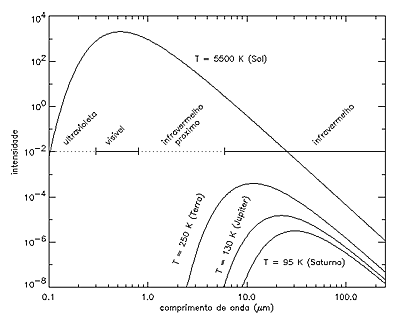 |
 |  Fig 1: Espectros de bolas de ferro a 4 temperaturas diferentes, correspondentes às temperaturas do Sol, da Terra, de Júpiter e de Saturno Fig 1: Espectros de bolas de ferro a 4 temperaturas diferentes, correspondentes às temperaturas do Sol, da Terra, de Júpiter e de Saturno |
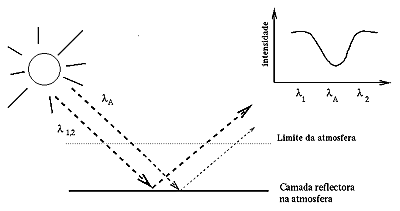
Um espectro é o resultado duma decomposição da luz: de todas as cores (comprimentos de onda) dos quais é composta a luz emitida ou reflectida por um astro determina-se a intensidade. Luz visível, que podemos imaginar como uma onda que se propaga com a velocidade da luz, tem comprimentos de onda (indicado pela letra grega  ) entre aproximadamente 0.3 e 0.8 micrómetros (1 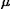 m = 1/1000 mm). O comprimento de onda determina a cor: luz azul tem um comprimento de onda por volta de 0.4 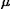 m, luz vermelho por volta de 0.7 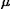 m. Chamamos à radiação de comprimentos de onda menores que 0.3 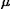 m, ultravioleta, raios-X ou gamma. Do outro lado temos a radiação infravermelha entre 1 e 1000 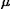 m, depois radiação milimétrica, e radio com comprimentos de onda de centímetros, metros, etc. . Um espectro é um diagrama da quantidade de radiação, a intensidade, emitida ou reflectida nos diferentes comprimentos de onda. A forma do espectro dum corpo celeste é influênciada pela sua temperatura. Tentemos compreender este efeito através dum fenónemo do dia à dia. Peguemos numa bola de ferro, e aqueçamo-la ao fogo. A bola vai mudar de cor, primeiro para um vermelho escuro, cada vez mais amarelo, e finalmente, quando a temperatura for muito alta, para um azul esbranquiçado. A temperatura da bola determina em que comprimento de onda a maior parte da radiação é emitida. O comprimento de onda para a qual o máximo da radição é emitida (  ) é mais pequeno (mais azul) quando a temperatura da bola é mais alta. Assim, pode-se determinar a temperatura da superfície duma estrela: estrelas azuis são mais quentes que estrelas vermelhas. A figura 1 mostra alguns espectros de bolas imaginárias, com diferentes temperaturas correspondentes às do Sol e de alguns planetas. Vemos que  para a bola de 5500 K vale 0.53 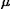 m, amarelo,enquanto que  da bola de 130 K se encontra no infravermelho, por volta de 22 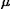 m. Também se nota que para temperaturas mais baixas, as intensidades em todos os comprimentos de onda são mais baixas. Se analisarmos um espectro do Sol, que tem uma temperatura de aproximadamente 5500 K à superfície, podemos confirmar que  max max é 0.53 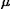 m, mas que além disso, o espectro tem muitas "quebras", onde de repente há muito menos radiação. Elas são a consequência da presença dos gases que constituem a atmosfera solar. Cada átomo, que constitui o gás, absorve radiação de comprimentos de onda muito específicos. A absorção é mais forte comforme a quantidade de gás que se encontra na atmosfera solar. Investigando o espectro de uma estrela, e conhecendo as características espectrais de diferentes átomos (por medidas feitas no laboratório) pode-se identificar a presença dum átomo na atmosfera estelar. Para as estrelas, por causa da alta temperatura da superfície, é na parte visível do espectro que encontramos a maior parte da informação. Uma outra diferença entre as atmosferas das estrelas e as dos planetas é que as últimas contêm moléculas em vez de átomos (só estrelas muito frias contêm algumas moléculas). A atmosfera terrestre é constituida principalmente de azoto(N ), oxigénio (O ), e pequenas quantidades de outros gases, como, por exemplo, o dióxido de carbono (CO ), a água (H O), e o metano (CH ). Por isso, o espectro de um planeta mostra muitas riscas e bandas largas de absorção, as impressões digitais das moléculas que constituem a sua atmosfera. Por serem constituidos por vários átomos, os espectros de moléculas são bastante complicados, mas, como no caso dos átomos, cada molécula tem o seu espectro característico. Espectros planetários Um espectro dum planeta consiste de duas partes: (1) a parte onde domina a radiação solar reflectida (  < 4 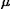 m), e (2) a parte onde a emissão térmica do planeta prevalece (  > 4 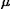 m). Falar em radiação reflectida implica a presença dum reflector. No caso da Terra pode ser a superfície (terra, mar) ou as nuvens. No caso de Júpiter, que não tem superfície sólida, são os topos das nuvens de amoníaco (figura 2). Se observarmos Júpiter no visível, vemos luz solar reflectida por esta camada de nuvens. Mas também por cima da camada há atmosfera. Imaginemos que a atmosfera é constituida por um tipo de molécula só, a molécula A. Esta molécula absorve fortemente radiação de comprimentos de onda  , mas não influencia a radiação de comprimentos de onda  e  .
 |  |
 | 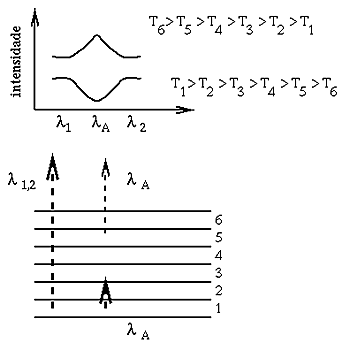 |
 |  Fig. 3: Formação duma banda de absorção para comprimentos de onda térmicos ( Fig. 3: Formação duma banda de absorção para comprimentos de onda térmicos (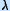 > 4 > 4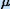 m) m) |
Na figura 2 vemos que a radiação solar de todos os comprimentos de onda faz o mesmo caminho. Porém, a radiação de  é absorvida em grande quantidade, e por isso a quantidade de radiação observada neste comprimento de onda, depois de ter atravessado a atmosfera, é menos que nos comprimentos de onda  e  . O resultado é a formação duma banda de absorção. A intensidade da absorção depende da maneira como a molécula A absorve (função do comprimento de onda), e da quantidade de atmosfera que a radiação solar tem de atravessar ( i.e. a profundidade da camada reflectora).A formação de bandas de absorção no infravermelho térmico (  > 4 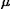 m) é feita da seguinte maneira. Na figura 3 dividimos a atmosfera em 6 camadas com diferentes temperaturas T - T . Imaginemos que a temperatura diminui quando a pressão diminui, i.e. quando a altitude aumenta; chama-se a esta parte da atmosfera a troposfera. Além disso imaginemos que a atmosfera é constituida por apenas uma mesma molécula, A, que absorve radiação de  (agora  é maior que 4 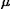 m). A radiação de  que provém das camadas mais profundas e quentes tem de atravessar muita atmosfera antes de sair, e encontra muitas moléculas A. Por isso, pouca desta radiação escapará da atmosfera. Pelo contrário, a radiação com  que provém das camadas mais altas e frias poderá escapar mais facilmente. Radiação com  e  não é absorvida pela molécula A, e mesmo a que vem das camadas profundas e quentes sairá para fora da atmosfera. Como se pode constatar pela figura 1, a temperatura e a intensidade da radiação emitida num dado comprimento de onda estão ligadas: mais baixa a temperatura, mais baixa a intensidade. Se metermos a intensidade da radiação que sai da atmosfera num diagrama em função do comprimento de onda, obtemos a curva na figura 3: uma banda de absorção. O mesmo tipo de raciocínio faz-se no caso duma estrutura térmica em que a temperatura aumenta com a altitude. Neste caso forma-se uma banda em emissão, porque a temperatura do nível do qual provém a radiação de  A A é mais alta e daí a intensidade ser mais alta também! A intensidade e a forma da banda não dependem só da quandidade do gás na atmosfera, e da maneira como as moléculas absorvem, mas também do perfil térmico. Para cálculos teóricos precisamos de saber pelo menos dois destes parâmetros para podermos determinar o outro, comparando os resultados teóricos com as observações. A maneira como a molécula absorve é algo que se pode medir no laboratório. É fácil de perceber que numa banda de absorção, desde o fundo da banda até ao bordo, se sondam diferentes níveis na atmosfera. Assim pode-se estudar a estrutura vertical da atmosfera. Por exemplo, sabendo a quantidade de gás e a sua distribuiçãovertical, pode-se determinar o perfil térmico, ou ao contrário.
|


 Os Space Scoops continuam a ser públicados, para consultar todos os disponiveis em Português pode seguir para a
Os Space Scoops continuam a ser públicados, para consultar todos os disponiveis em Português pode seguir para a